|
| Preparando un plaguicida..! |
- Arsenicales.
- Carbamatos.
- Derivados de cumarina.
- Derivados de urea.
- Dinitrocompuestos.
- Organoclorados.
- Organofosforados.
- Organometálicos.
- Piretroides.
- Tiocarbamatos.
- Triazinas.
A partir de cloro
Los alcanos y arilalcanos pueden ser tratados con cloro en condiciones libres de radicales, con luz UV. Sin embargo, el grado de cloración es difícil de controlar. Los cloruros de arilo pueden ser preparados mediante la halogenación de Friedel-Crafts, usando cloro y un ácido de Lewis como catalizador.La reacción del haloformo, usando cloro e hidróxido de sodio, también es capaz de generar halogenuros de alquilo a partir de metilcetonas y compuestos relacionados. El cloroformo se produjo antiguamente de esta manera.
El cloro sufre reacciones de adición a los enlaces múltiples como en alquenos, alquinos y otros, dando a compuestos di, tri o tetra-clorados.
Reacción con cloruro de hidrógeno
Los alquenos reaccionan con el cloruro de hidrógeno (HCl) para dar cloruros de alquilo. Por ejemplo, la producción industrial de cloroetano procede de la reacción del etileno con HCl:- H2C=CH2 + HCl → CH3CH2Cl
Otros agentes de cloración
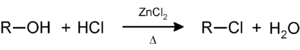
En el laboratorio, los cloruros de alquilo son más fáciles de preparar por reacción de alcoholes con cloruro de tionilo (SOCl2), tricloruro de fósforo (PCl3), o pentacloruro de fósforo (PCl5):- ROH + SOCl2 → RCl + SO2 + HCl
- 3 ROH + PCl3 → 3 RCl + H3PO3
- ROH + PCl5 → RCl + POCl3
- No utilizar plaguicidas clorados en las proximidades de llamas abiertas u objetos incandescentes, debido al peligro de descomposición que presentan, con formación de monóxido de carbono, cloruro de hidrógeno y fosgeno. Por igual razón, abstenerse de fumar en presencia de dichos productos.
- No reutilizar botellas de agua o contenedores de bebidas, rellenándolos con los productos en cuestión ni rellenar los envases de plaguicidas con agua o bebidas.
- Evitar el contacto de estos productos con álcalis, oxidantes fuertes y metales en general.
- En caso de duda, consultar la ficha de seguridad de cada producto en particular.
- Elegir el producto adecuado.
- Leer atentamente las instrucciones de uso contenidas en la hoja de seguridad.
- Respetar las dosis recomendadas.
- Extremar las precauciones durante la preparación de la mezcla de los productos a aplicar, ya que se trabaja con principios activos concentrados.
- Revisar todo el equipo de aplicación, para no trabajar con aparatos defectuosos.
- Llevar siempre el equipo de protección adecuado que se indica en la hoja de seguridad del producto. Como norma general y dada su toxicidad, deben usarse las siguientes medidas de protección personal para:
- Cabeza:Cubrirla con sombrero de ala ancha o gorra.
- Nariz y boca: Mascarilla totalmente ajustada.
- Manos y piel en general: Utilizar guantes.
- Pies:Botas de goma altas, con los pantalones por encima. Nunca utilice sandalias o alpargatas.
- Cuerpo en general: Ropa de trabajo con las mangas largas y ceñidas en las muñecas y las perneras en los tobillos. Utilizar mandil impermeable.
- Comenzar utilizando siempre ropa lavada y prendas de protección limpias.
- No comer, beber ni fumar, ni mantener alimentos o bebidas en la zona de trabajo.
- No limpiar las boquillas de aplicación soplando.
- Lavarse las manos antes de ir a orinar, ya que muchos de estos productos se absorben por las mucosas genitales provocando lesiones.
- Cuando se realice algún descanso, hacerlo siempre fuera de la zona tratada.
- Aplicar siempre a favor del viento.
- Evitar que las personas no ajenas a la aplicación estén en la zona de trabajo.
- Extremar la higiene personal, duchándose y cambiándose de ropa al terminar el trabajo. Separar adecuadamente la ropa de trabajo de la de calle, evitando que se mezclen. La ropa contaminada debe guardarse bien cerrada hasta su lavado, que debe hacerse separada del resto.
- No permanecer ni entrar en la zona tratada hasta, como mínimo, 48 horas después del tratamiento o del tiempo que se especifique en la etiqueta.
- Mantener el plaguicida sobrante en su envase original, almacenado en lugar fresco, seguro y ventilado y fuera del alcance de niños y personas que desconozcan sus riesgos.